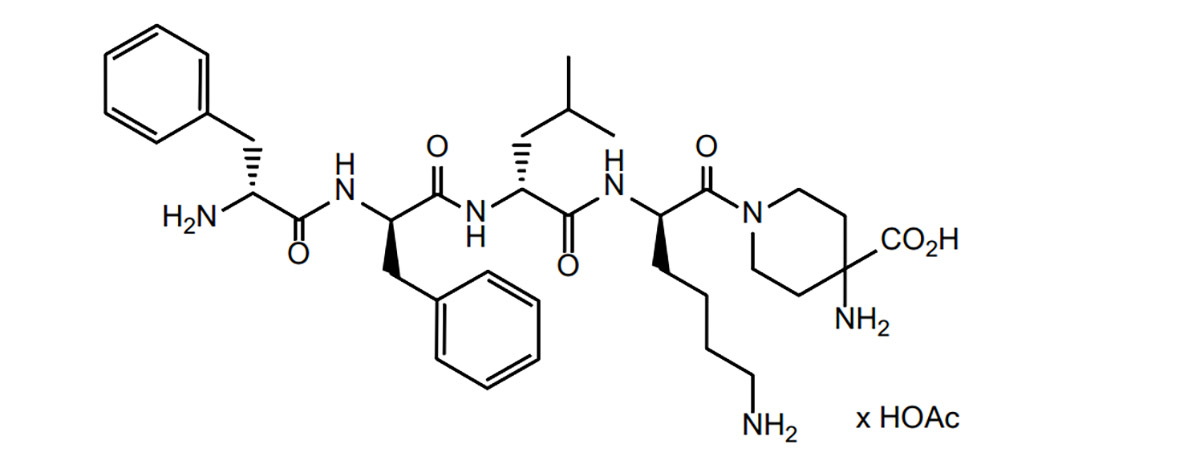
2021年8月24日、Cara TherapeuticsとそのビジネスパートナーであるVifor Pharmaは、同社のファーストインクラスのκオピオイド受容体作動薬ジフェリケファリン(KORSUVA™)が慢性腎臓病(CKD)患者(血液透析治療中の中等度/重度の掻痒陽性)の治療薬としてFDAの承認を取得し、2022年第1四半期に発売される予定であると発表しました。CaraとViforは、米国におけるKORSUVA™の商業化に関する独占ライセンス契約を締結し、KORSUVA™をFresenius Medicalに販売することに合意しました。このうち、CaraとViforは、Fresenius Medical以外の売上高について、それぞれ60%と40%の利益分配を持ち、Fresenius Medicalからの売上高については、それぞれ50%の利益分配を持ちます。
CKD関連掻痒症(CKD-aP)は、透析を受けているCKD患者に高頻度かつ高強度で発症する全身性掻痒症です。透析を受けている患者の約60%~70%に掻痒が見られ、そのうち30%~40%は中等度/重度の掻痒を呈し、生活の質(睡眠の質の低下など)に深刻な影響を与え、うつ病にも関連しています。これまでCKD関連掻痒症に対する効果的な治療法はなく、ジフェリケファリンの承認は、この大きな医療ニーズのギャップを埋める一助となります。今回の承認は、NDA申請における2つの重要な第III相臨床試験、すなわち米国および世界各国で実施されたKALM-1試験およびKALM-2試験の肯定的なデータ、およびKORSUVA™の良好な忍容性を実証する32の追加臨床試験の裏付けデータに基づいています。
少し前に、ジフェリケファリンの日本での臨床試験から朗報が届きました。2022年1月10日、Caraは、パートナーである丸石製薬とキッセイファーマが、ジフェリケファリン注射剤が日本で血液透析患者の掻痒の治療に使用されていることを確認したと発表しました。第III相臨床試験で主要評価項目が達成されました。178人の患者が6週間のジフェリケファリンまたはプラセボを投与され、52週間のオープンラベル延長試験に参加しました。主要評価項目(掻痒数値評価尺度スコアの変化)と副次評価項目(白鳥重症度スケールによる掻痒スコアの変化)は、プラセボ群と比較して、ジフェリケファリン群でベースラインから有意に改善し、忍容性も良好でした。
ジフェリケファリンはオピオイドペプチドの一種です。これに基づき、ペプチド研究所はオピオイドペプチドに関する文献を調査し、医薬品開発におけるオピオイドペプチドの課題と戦略、そして現在の医薬品開発状況をまとめました。
投稿日時: 2022年2月17日